연구자 의뢰자 지원
절차 안내
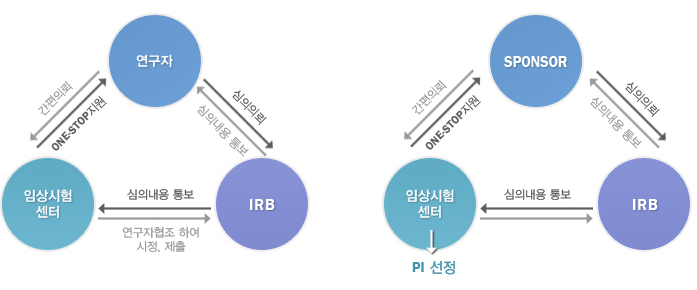
임상시험센터 임상연구 지원 절차 안내
- STEP01 임상시험 지원 신청
ctc@gilhospital.com - STEP02 임상시험 지원 여부 검토
(통상적으로 1~2주 소요) - STEP03 지원 여부 및 지원 범위 결정
(지원협약서 작성)
임상시험
시작 단계

| STEP01 | 임상시험계획서 |
|---|---|
| STEP02 | 증례기록서(Clinical report form) 검토 |
| STEP03 | 시설 및 부서 협조 절차 조정 |
| STEP04 | 사전 교육 |
| STEP05 | 근거 문서 준비 |
| STEP06 | 임상시험관련 물품 수령 및 보관 |
| STEP07 | 개시 모임 준비 및 참여 |
| STEP08 | 임상시험 의약품 수령 및 보관 확인 |
임상시험
수행 단계

| STEP01 | 잠재 피험자 모집, 서면 동의 취득 |
|---|---|
| STEP02 | 잠재 피험자 스크리닝 및 피험자 등록, 무작위 배정 |
| STEP03 | 시험 처치, 연구 자료 수집, 증례기록서 작성 |
| STEP04 | 피험자 관찰 및 보고 : 치료반응 및 이상반응 |
| STEP05 | 피험자 유지 및 관리 |
| STEP06 | 임상시험에 사용하는 의약품 관리, 문서 관리 |
| STEP07 | 의뢰자 모니터링, AUDIT준비 |
임상시험
종료 단계

| STEP01 | 증례기록서 작성 완료 |
|---|---|
| STEP02 | 임상시험관련 물품 처리 |
| STEP03 | 임상시험에 사용하는 의약품 처리 |
| STEP04 | 연구비 정산 및 종료 보고 |
| STEP05 | 실태조사(inspection) 준비 및 참여 |
| STEP06 | 연구 결과 보고서 IRB에 보고 |
| STEP07 | 문서 보관 |
연구자 의뢰자
이용안내
- STEP01 신청서 작성
- STEP02 센터제출
- STEP03 센터 이용비
산정 및 협의 - STEP04 센터이용
- STEP05 센터이용비
납부
☎ 임상시험센터 문의 : 032-460-9460
